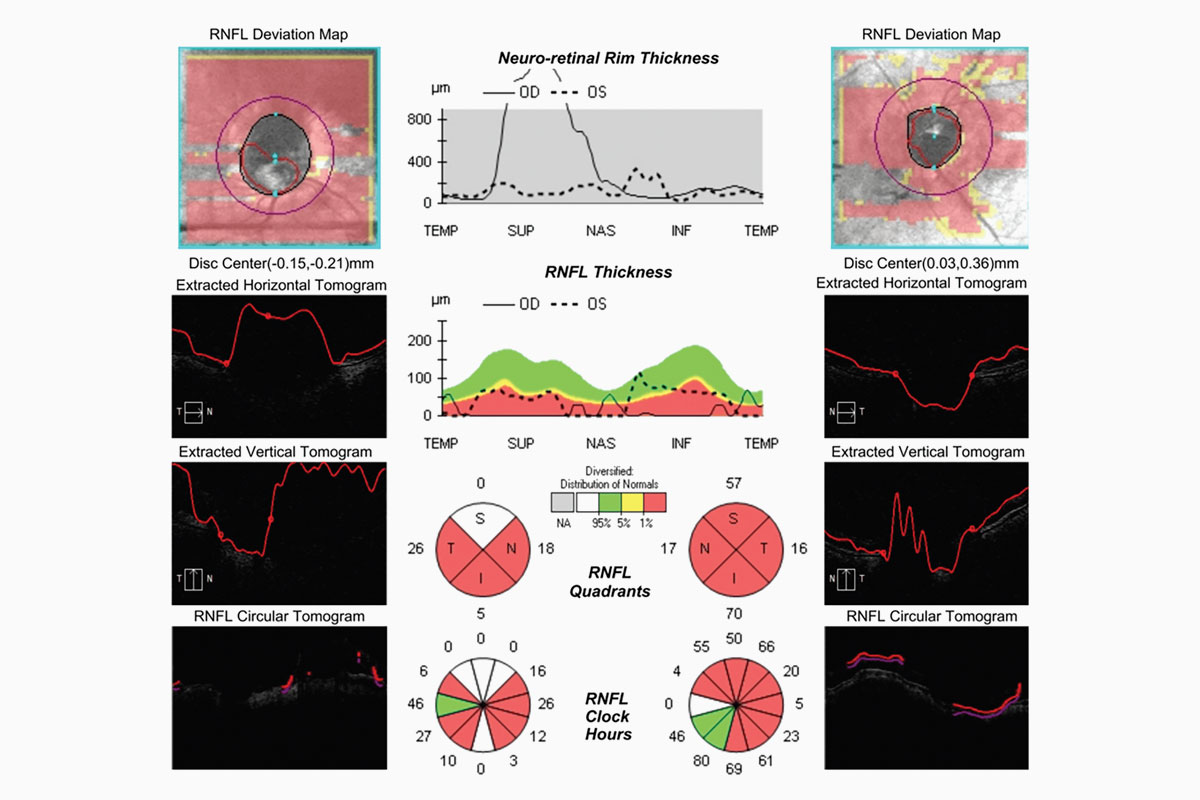
El manejo de la catarata hipermadura representa un desafío quirúrgico mayor debido al riesgo incrementado de complicaciones, como la ruptura capsular posterior o la descompensación corneal. Este escenario se magnifica considerablemente en ojos que presentan compromiso endotelial y una ampolla de filtración funcionante por trabeculectomía previa.
La elección del abordaje quirúrgico representa la primera gran interrogante ante este escenario. Al comparar la pérdida endotelial entre la facoemulsificación y otras técnicas manuales como la cirugía manual de pequeña incisión (MSICS) o la extracción extracapsular de catarata (ECCE), la literatura ofrece perspectivas divergentes, usualmente evaluadas a las seis semanas postoperatorias. Por un lado, Ganekal y Nagarajappa reportaron resultados favorables para la facoemulsificación en un estudio aleatorizado (n=200). En su serie, dicho grupo mostró una pérdida celular significativamente menor frente a la técnica de MSICS: 76.12 células/mm² (3.27%) y 315.08 células/mm² (13.49%), respectivamente (1).
En contraste, Gogate y colaboradores no hallaron diferencias estadísticas utilizando un sistema de conteo de células manual y automatizado en la microscopía especular. El método manual reportó una pérdida de 543.4 células/mm² en facoemulsificación vs. 505.9 en MSICS (P=0.44), mientras que el automatizado mostró 474.2 vs. 456.1, respectivamente (P=0.98) (2). Asimismo, un estudio comparativo entre ECCE convencional, MSICS y facoemulsificación no encontró variaciones significativas, con descensos en el recuento celular de 4.72%, 4.21% y 5.41%, respectivamente (3). Finalmente, Singh y colaboradores evidenciaron una ventaja para la MSICS, con una pérdida menor (201.2 ± 158.2 células/mm²) frente a la facoemulsificación (334.3 ± 253.2; P=0.0071). Adicionalmente, el estudio reveló un punto crítico: un umbral inferior a 2.86 mm en la profundidad de la cámara anterior se correlacionó con una pérdida significativamente mayor de células durante la facoemulsificación (4).
Desde una perspectiva refractiva, la elección de la técnica también resulta determinante. Mientras la ECCE convencional suele inducir un astigmatismo “contra la regla” significativo y errático, la arquitectura del túnel escleral en la MSICS proporciona una estabilidad óptica que se aproxima a la facoemulsificación. Al respecto, George et al. (4) reportaron un astigmatismo inducido (SIA) de 1.77 ± 1.61 D para el grupo de ECCE, frente a 1.17 ± 0.95 D en MSICS y 0.77 ± 0.65 D en facoemulsificación (P=0.001). Si bien la diferencia de magnitud entre MSICS y facoemulsificación fue de apenas 0.4 D, dicha brecha no parece impactar drásticamente el éxito visual final. Esto coincide con lo reportado por Gogate et al. (3), quienes a las seis semanas no hallaron diferencias clínicas significativas en la agudeza visual corregida (mejor a 6/18) entre ambos grupos: 98.5% para facoemulsificación y 97.3% para MSICS.
La preservación de la función filtrante es prioritaria, dado que la cirugía de catarata eleva el riesgo de falla de la trabeculectomía, especialmente en intervalos postoperatorios breves entre una cirugía y otra (5). Siriwardena et al. sugieren que la fibrosis en la interfase conjuntiva-escleral es la principal barrera para una filtración efectiva. La inflamación secundaria a la liberación de proteínas, los altos volúmenes de irrigación y, crucialmente, la energía ultrasónica, disparan la producción de citoquinas fibrogénicas en el humor acuoso (6). Por tanto, la MSICS se presenta como una alternativa estratégica al eliminar el trauma térmico y vibratorio del ultrasonido, factores que de otro modo promoverían la cicatrización del sitio quirúrgico previo.
Más allá de la técnica, el éxito en escenarios complejos exige una planificación preoperatoria rigurosa. Esta inicia con la clasificación de la nucleoesclerosis y su impacto funcional, pero el RCE es el mandato absoluto para evaluar la reserva biológica. Un recuento bajo (<1000 células/mm²) obliga a considerar la MSICS, una facoemulsificación ultracorta o, ante una descompensación inminente, cirugía combinada con trasplante endotelial (DMEK/DSAEK). En este contexto, la paquimetría es un indicador clave: grosores superiores a 600 µm suelen ser la primera señal de una disfunción endotelial preexistente (7).
Aplicación clínica: Un desafío en la práctica real
Presentamos el caso de una paciente de 81 años con agudeza visual de ‘cuenta dedos’ en el ojo derecho y antecedente de trabeculectomía, cuya ampolla filtrante superior se encontraba funcional, pero marcadamente adelgazada (Figuras 1 y 2).
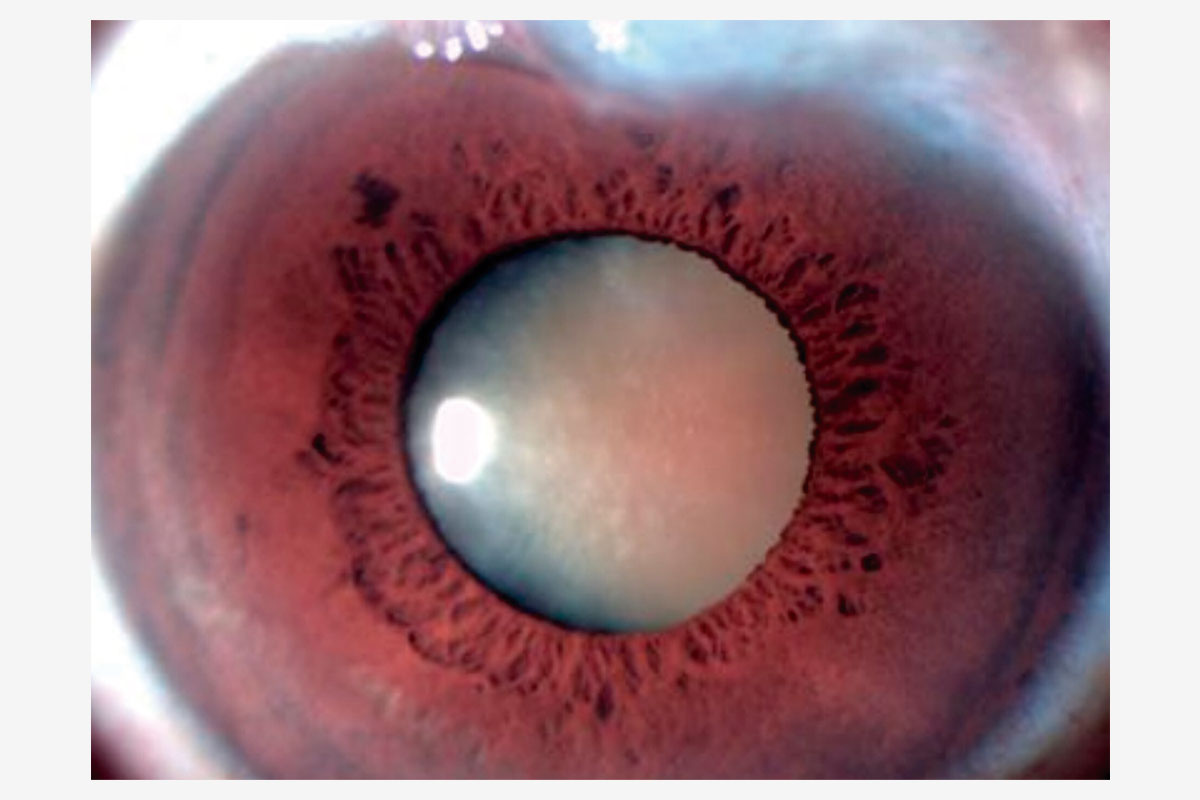
Figura 1. Catarata hipermadura
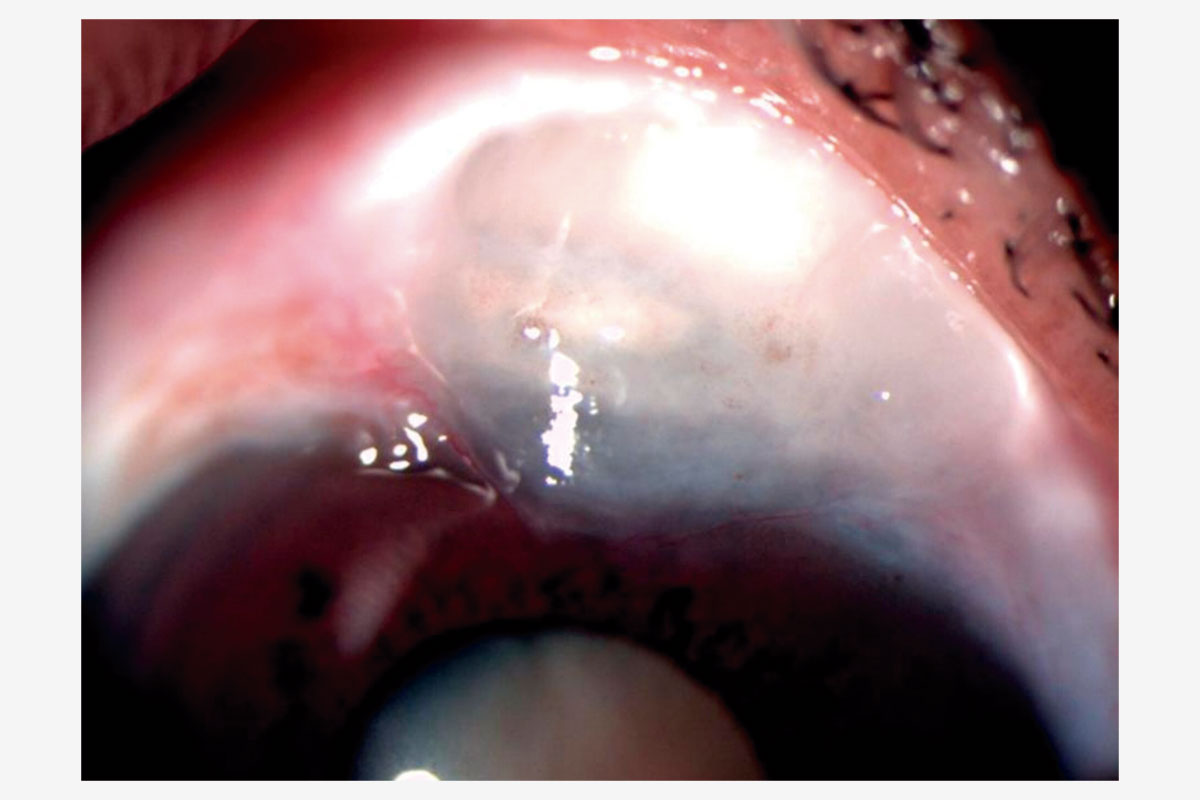
Figura 2. Ampolla filtrante avascular y adelgazada
A la exploración, destacaba una catarata hipermadura, PIO de 9 mmHg y daño glaucomatoso avanzado (copa/disco 0.9). La estrategia quirúrgica se definió mediante la microscopia especular y la UBM: un RCE crítico de 997 células/mm² (Figura 3) y un cristalino de gran diámetro anteroposterior con lens vault aumentado (Figura 4).
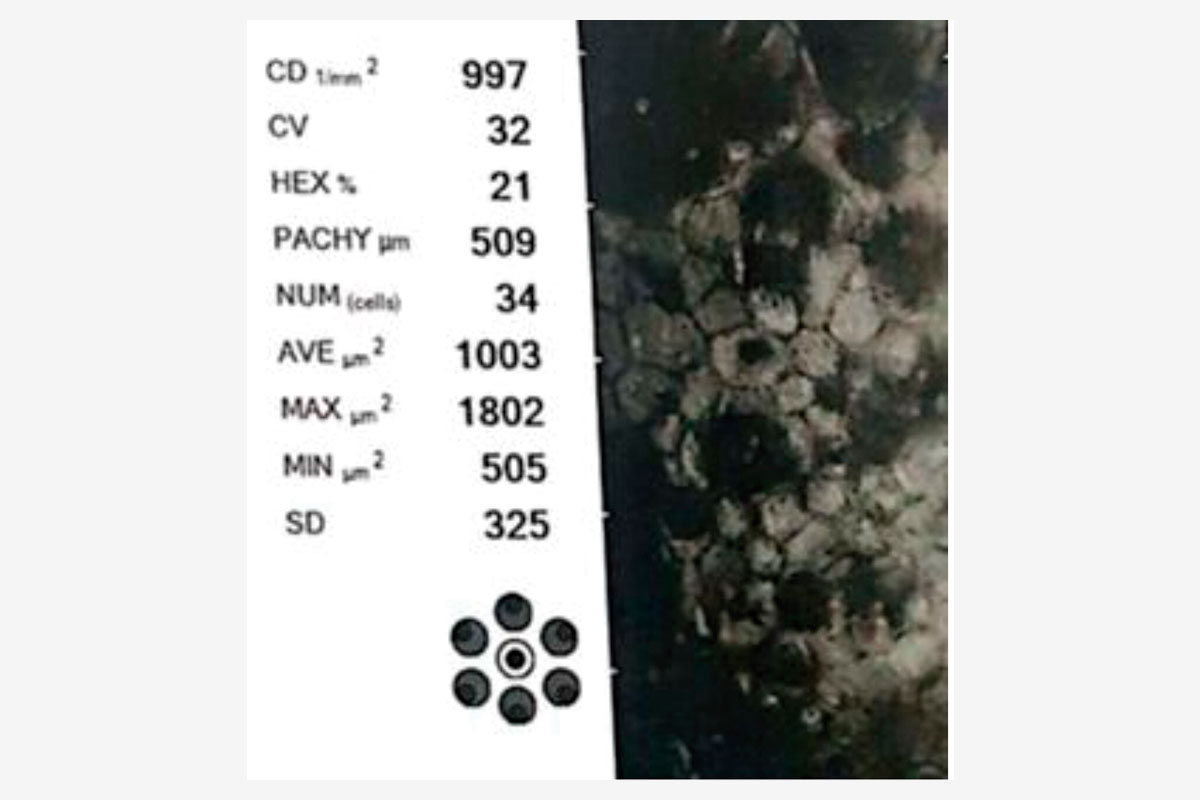
Figura 3. Microscopia especular preoperatoria

Figura 4. UBM mostrando catarata con aumento del diámetro AP y del lens vault
La decisión quirúrgica
Ante este escenario, donde la dureza nuclear y la estrechez del espacio de maniobra hacían de la facoemulsificación una opción de alto riesgo para el endotelio, se optó por una MSICS con abordaje temporal para minimizar el riesgo endotelial y proteger la ampolla filtrante superior. Se confeccionó un túnel escleral de 7 mm para una extracción del núcleo sin estrés mecánico (Figura 5). Se implantó una lente intraocular de tres piezas bajo viscoelástico y se aseguró la hermeticidad con un único punto corneoescleral (Figura 6).

Figura 5. Túnel escleral de la MSICS

Figura 6. Sutura del túnel escleral con un punto de nylon
Resultados y evolución
El resultado postoperatorio validó la elección de la técnica. La paciente alcanzó una mejoría visual significativa, pasando de cuenta dedos a 20/40. En el seguimiento, se observó la lente centrada, el túnel sellado y una PIO estable de 9 mmHg (Figura 7A). La ampolla filtrante permaneció funcional y sin cambios morfológicos respecto al estado preoperatorio (Figura 7B).
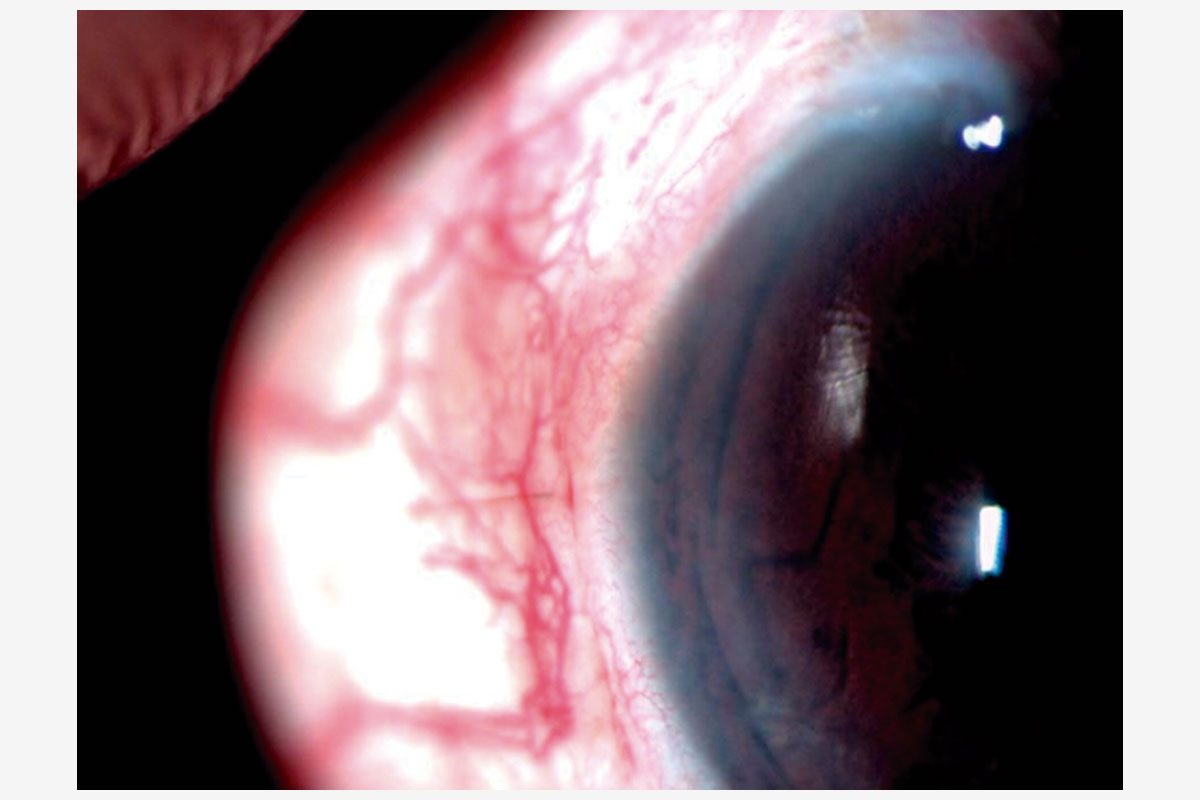
Figura 7A. Conjuntiva temporal en el postoperatorio
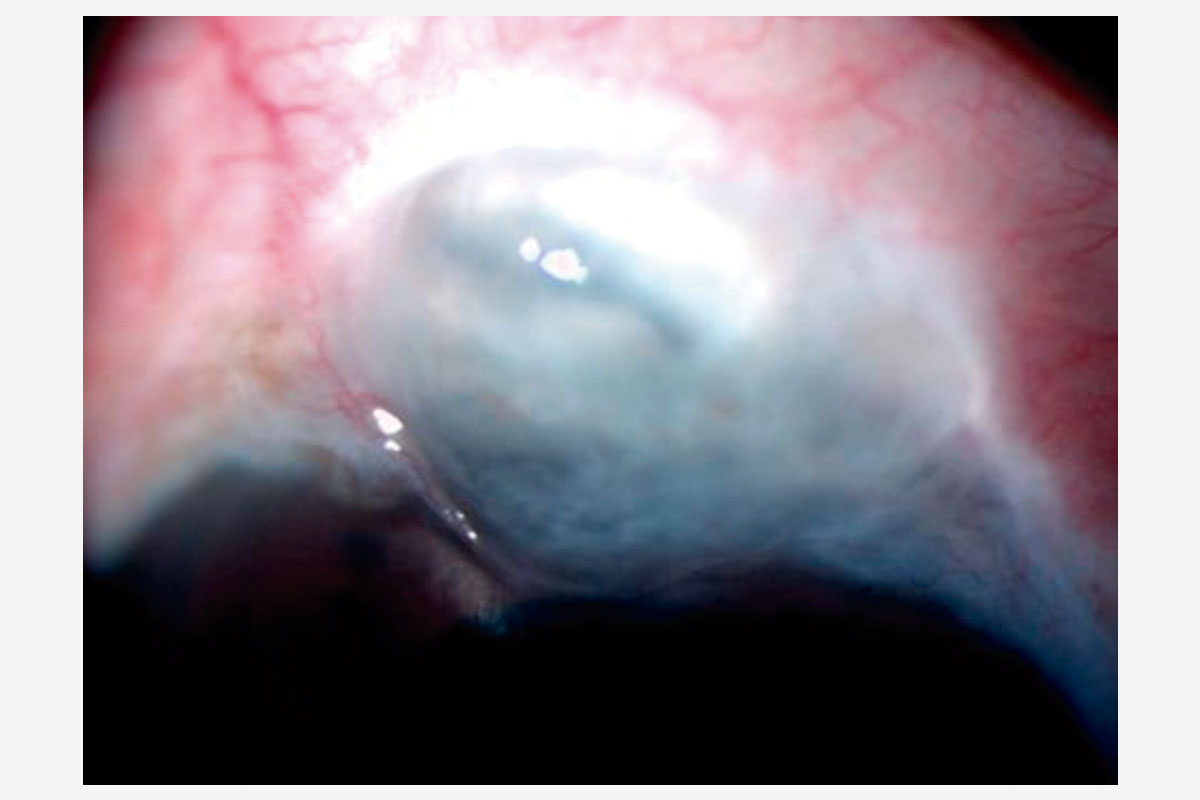
Figura 7B. Ampolla filtrante posterior a MSICS
Conclusión
El manejo de la catarata hipermadura en un ojo con RCE bajo y una trabeculectomía previa es una cirugía de alto riesgo que demanda la máxima pericia del cirujano. El éxito depende de una planificación preoperatoria detallada, la comprensión de la anatomía alterada y el empleo de técnicas quirúrgicas que minimicen la energía ultrasónica y la manipulación endotelial, a la vez que se protege la integridad y función de la ampolla de filtración. El cuidado postoperatorio secuencial es esencial para mantener la transparencia corneal, el control de la PIO y la funcionalidad de la trabeculectomía.
Referencias:
Ganekal S, Nagarajappa A. Comparison of morphological and functional endothelial cell changes after cataract surgery: Phacoemulsification versus manual small-incision cataract surgery. Middle East Afr J Ophthalmol 2014;21:56-60
Gogate P, Ambardekar P, Kulkarni S, Deshpande R, Joshi S, Deshpande M. Comparison of endothelial cell loss after cataract surgery: phacoemulsification versus manual small-incision cataract surgery: six-week results of a randomized control trial. J Cataract Refract Surg. 2010;36(2):247-53
George R, Rupauliha P, Sripriya AV, Rajesh PS, Vahan PV, Praveen S. Comparison of endothelial cell loss and surgically induced astigmatism following conventional extracapsular cataract surgery, manual small-incision surgery and phacoemulsification. Ophthalmic Epidemiol. 2005;12(5):293-7
Singh R, Sharma AK, Katiyar V, Kumar G, Gupta SK. Corneal endothelial changes following cataract surgery in hard nuclear cataract: Randomized trial comparing phacoemulsification to manual small incision cataract surgery. Indian J Ophthalmol 2022;70:3904-9.
Husain R, Liang S, Foster PJ, et al. Cataract surgery after trabeculectomy: the effect on trabeculectomy function. Arch Ophthalmol. 2012;130(2):165-170
Sirwardena D, Kotecha A, Minassian D, et al. Anterior chamber flare after trabeculectomy and after phacoemulsification. Br J Ophthalmol. 2000;84:1056-1057
Dada T, Bhartiya S, Begum Baig N. Cataract Surgery in Eyes with Previous Glaucoma Surgery: Pearls and Pitfalls. J Curr Glaucoma Pract. 2013 Sep-Dec;7(3):99-105
Únase a Glaucoma Colombia y forme parte de una comunidad comprometida con la salud ocular y la concientización sobre el glaucoma, impulsando el cuidado ocular y la investigación. https://www.glaucomacolombia.org/membresias/